我們阻止不了年歲增長,但可以決定細胞發電廠的效能,重置生理年齡。
2013年,國際知名學術期刊《Cell》發表的〈The Hallmarks of Aging〉(老化的特徵),首次系統性提出老化的九大特徵,粒線體功能障礙(Mitochondrial Dysfunction)即被列為其中之一。2025年,老化特徵已擴增至14項,粒線體功能障礙歸類於拮抗型特徵。
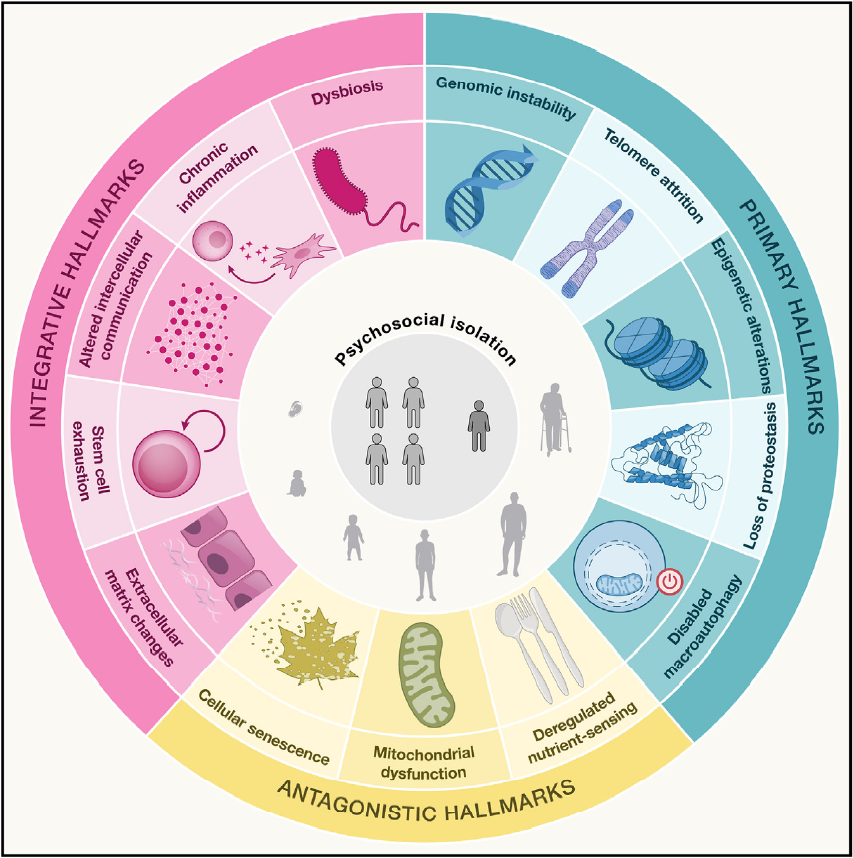
2025年最新發佈的14項老化特徵(圖片來源:Cell. 2025 Apr 17;188(8):2043-2062.)
關於粒線體與老化的關聯,可溯至1950年代美國科學家哈曼(Denham Harman)提出的「自由基假說」,他認為在細胞正常代謝過程中,粒線體產生過量的活性氧(ROS)會引起細胞氧化損傷,並影響粒線體功能,致使細胞能量(ATP)生成減少,奠下老化根基。
粒線體會隨著年齡增加而功能失調,而隨著粒線體功能下降,可以觀察到器官功能衰退,並與癌症、心血管疾病和神經退化性疾病等多種老化相關疾病的發生相關。優化粒線體(Mitochondria Optimization)是目前最被看好的有效抗老化對策之一,從優化細胞能量工廠著手,以汰舊(清除受損粒線體)與換新(製造新的粒線體)來強化粒線體功能,賦予細胞滿滿年輕又健康的活力。
粒線體是一個寄生於細胞的獨立生物體?
粒線體的主要功能是,將細胞攝入的營養轉換成細胞可以使用能量(ATP),以維持身體器官正常運作,因而又有「細胞發電廠」或「細胞能量工廠」之稱。一個正常細胞含數個至數千個或更多的粒線體,其數量與細胞的代謝效率成正比,比如腦細胞、心肌細胞、肝細胞、骨骼肌細胞等耗能大戶,代謝活動繁忙,粒線體密度就高。此外,粒線體也參與訊息傳遞、代謝調控與細胞凋亡等過程。
有別於細胞核DNA,粒線體擁有自己的小型環狀DNA(mtDNA),共攜帶37個基因,由母親遺傳而來,負責製造本身所需的蛋白質。細胞內共生理論曾提出的一個有趣的觀點,粒線體是細胞內獨立的生物體,可能是細菌被原始真核細胞吞噬後,形成互利共生關係,歷經長時間演化,最終變成細胞的獨立胞器。
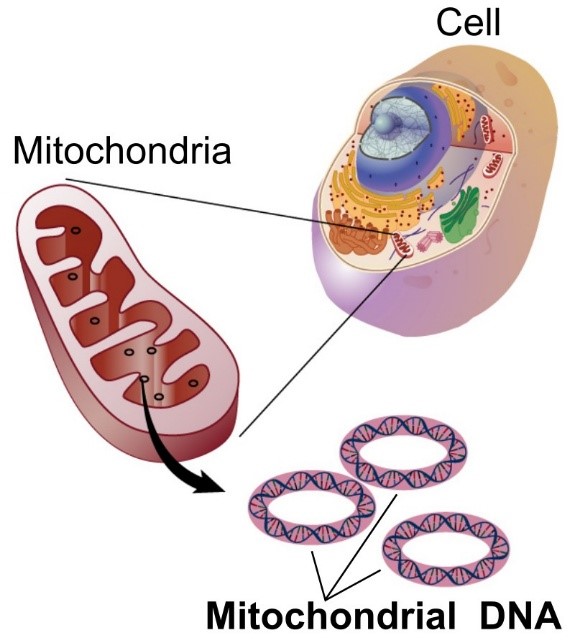
(圖片來源:Wikipedia)
粒線體與端粒體,傻傻分不清?
粒線體(mitochondria)與端粒體(telomere),是細胞中兩個攸關細胞老化速度和凋亡的重要胞器。粒線體是細胞的能量工廠,負責產生能量(ATP);而端粒體則是染色體末端的保護帽,與遺傳相關,長度會隨著細胞分裂而縮短。兩者功能不同,但存在著密切的聯繫,粒線體產生的ROS會損傷端粒體,而端粒體功能障礙也會影響粒線體的功能,兩者都會導致老化。
老化加速器:粒線體功能障礙
粒線體是調節能量和代謝穩態的核心,一旦失調經常會導致病理性的變化。粒線體功能障礙會引發一連串連鎖反應,包括氧化和抗氧化失衡、粒線體動態失衡、粒線體DNA損傷和粒線體自噬作用受損等,進而導致氧化壓力和發炎反應,最終對老化產生關鍵影響。
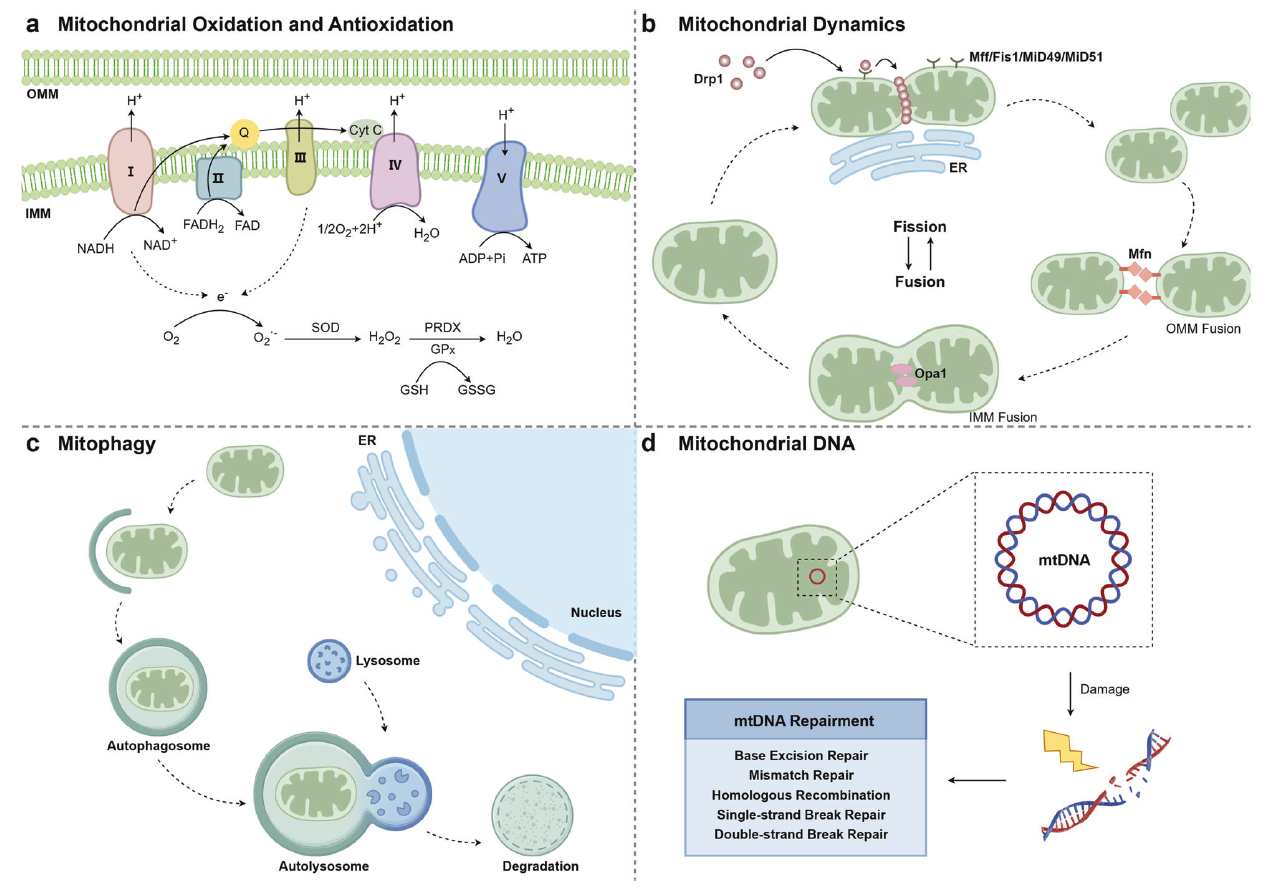
粒線體功能障礙包括氧化和抗氧化失衡、粒線體動態失衡、粒線體DNA損傷以及粒線體自噬受損(圖片來源:Signal Transduct Target Ther. 2025 Jun 11;10(1):190.)
影響1. 氧化和抗氧化失衡
粒線體在產能過程中所產生的副產物──活性氧(ROS),是自由基的一種,也是細胞內最主要的ROS來源。當粒線體產生的ROS超出抗氧化酵素系統的清除能力時,會導致氧化壓力上升,破壞細胞內的脂質、蛋白質和DNA等重要結構,造成細胞損傷,甚至誘發細胞凋亡。粒線體產生的ROS也會攻擊粒線體,導致粒線體功能障礙,進而產生更多的ROS,形成惡性循環,驅動老化。
能量是細胞生命活動的基礎,驅動維持生命所需的各種過程。若氧化壓力損害粒線體功能,導致無法產出足夠的ATP供給細胞進行生命運作,細胞便會提早老化甚或死亡,腦、心、肝等高耗能器官將最先受害。
影響2. 粒線體動態失衡
粒線體在特定條件下可以動態地融合或分裂,賦予粒線體不同的形態,並影響粒線體的數量和品質,進而影響細胞的代謝和功能。正常情況下,適當的融合與分裂可去除受損的粒線體並維持細胞穩態;這個動態一旦失衡,粒線體過度分裂或融合不足,會導致功能異常的粒線體的累積。過多的受損粒線體會促進ROS過度產生,影響粒線體自噬,加速細胞功能衰退。
影響3. 粒線體DNA損傷
粒線體擁有獨立的基因組(mtDNA),對維持粒線體功能至關重要。由於mtDNA鄰近ROS產生的區域且缺乏完善的保護,它比細胞核DNA更容易受到氧化損傷,使得mtDNA突變率增加,進一步加重粒線體功能障礙。雖然粒線體有修復mtDNA氧化損傷的能力,但隨著年齡增長,mtDNA損傷累積仍難以避免。此外,氧化壓力與mtDNA損傷互為因果:ROS會造成mtDNA損傷,而受損mtDNA又會加劇ROS的產生,形成惡性循環。
影響4. 粒線體自噬受損
粒線體自噬是細胞清除受損粒線體以維持穩態的關鍵機制。細胞在遭受氧化壓力時,會啟動粒線體的自噬作用。適度增強粒線體的自噬作用,有助排除受損粒線體、降低ROS並保護細胞;反之,若粒線體的自噬作用失靈,受損的粒線體無法被及時清除,堆積的受損粒線體會導致更多的ROS累積,致使細胞損傷甚至死亡。
粒線體功能障礙會加重慢性發炎
慢性低度發炎也是加速老化的重要推手,這種現象被稱為發炎性老化(inflammaging)。發炎時所釋放的細胞激素會造成組織損傷,持續積累的損傷會推動老化進展。粒線體在老化相關的發炎反應亦扮演關鍵角色。當粒線體功能障礙時,粒線體會釋放mtDNA和ROS等分子,活化發炎小體,並化身為損傷相關分子模式(DAMPs),啟動免疫反應。此外,粒線體功能障礙也會影響嗜中性球、巨噬細胞和T細胞等免疫細胞的功能,透過多種途徑促進發炎反應。氧化壓力和發炎已被證實參與老化過程,如此一來,粒線體功能障礙既是老化的直接因素,也是間接因素。
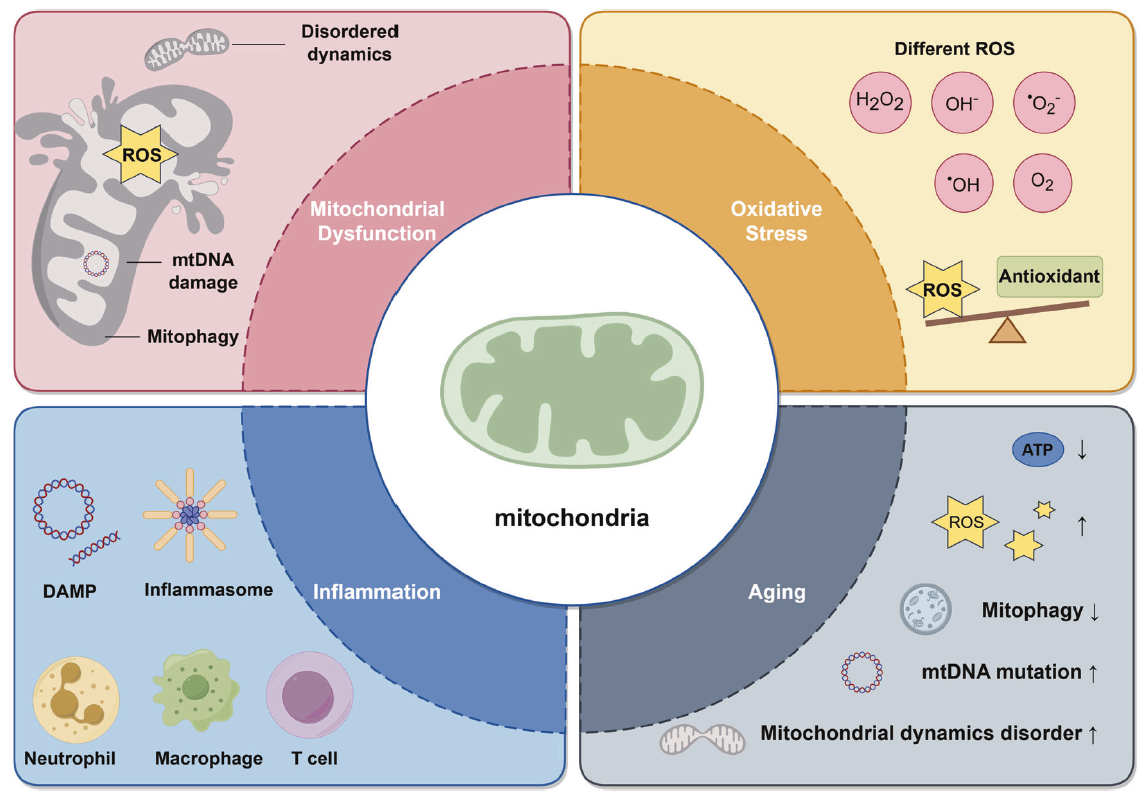
粒線體是連結發炎、氧化壓力和老化的核心(圖片來源:Signal Transduct Target Ther. 2025 Jun 11;10(1):190.)
粒線體:連結發炎、氧化壓力和老化的關鍵樞紐
粒線體既是ROS產生的主要場所,也是清除ROS的核心平台。粒線體功能障礙往往會引起ROS累積、氧化壓力上升,同時觸發發炎反應,氧化壓力與發炎反應因此往往相伴出現。兩者在長期交互作用之下會損害粒線體功能,並形成惡性循環,最終對組織、器官造成損傷並加速老化。粒線體功能障礙、氧化壓力和發炎,三者相互促進,構成老化相關病理的關鍵樞紐。
粒線體優化對策
粒線體是調節氧化壓力、發炎和老化的關鍵。改善粒線體,有望同時緩解這三方面的異常。
|
策略 |
具體項目 |
主要機制與效益 |
備註 / 臨床應用 |
|
1. 運動與飲食 |
運動 |
增加ATP消耗 → 提升電子傳遞鏈速度,促進粒線體分裂與 |
|
|
垂直律動儀 |
高頻小幅度垂直機械震動 → 模擬肌肉收縮,活化粒線體代謝與產能 |
適合無法高強度運 |
|
|
飲食策略(熱量限制/斷食/生酮) |
促進粒線體自噬、粒線體分裂和融合的平衡 |
||
|
2. 營養素與 |
抗氧化劑 |
輔酶Q10:標靶進入粒線體,降低氧化壓力,保護DNA |
針對氧化損傷防護 |
|
自噬調控因子 |
活化粒線體自噬 → 清除受損粒線體,降低ROS與發炎反應 |
|
|
|
3. 光療法 |
光生物調節 |
照射600-1000nm紅光 → 活化電子傳遞鏈樞紐:細胞色素C氧化酶 → 提升ATP產能效率 |
提升細胞活力 |
|
4. 溫度調控 |
冷暴露 |
提升粒線體數量與活性 → 產熱活化棕色脂肪、 |
|
|
熱壓力 |
血管擴張、改善灌流,促進粒線體生成與能量轉換 |
||
|
5. 特殊療法 |
脈衝電磁場(PEMF) |
利用脈衝磁場來改變膜電位 → 降低氧化壓力,促進粒線體更新,提升ATP產能 |
非侵入性物理治療 |
|
間歇性低氧/高氧 (IHHT) |
低氧/高氧循環交替 → 透過粒線體自噬清除受損的粒線體 |
||
|
6. 前瞻療法 |
粒線體移植 |
將健康粒線體植入受損組織 |
目前需更多臨床安全性試驗 |
參考資料: